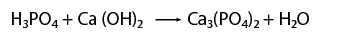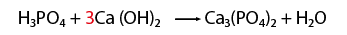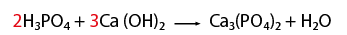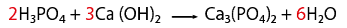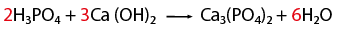Balanceo
El balanceo consiste en igualar el número de átomos de cada elemento tanto en los reactivos como en los productos, y sirve para verificar la Ley de la Conservación de la Materia (La materia no se crea ni se destruye solo se transforma).
Para escribir y balancear una ecuación química de manera correcta, es necesario tener presente las siguientes recomendaciones:
- Revisar que la ecuación química esté completa y correctamente escrita.
- Observar si se encuentra balanceada.
- Balancear primero los metales, los no metales y al final el oxígeno y el hidrógeno presentes en la ecuación química.
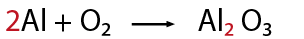
- Escribir los números requeridos como coeficiente al inicio de cada compuesto.
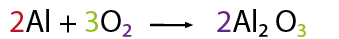
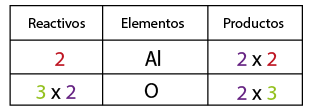
- Contar el número de átomos multiplicando el coeficiente con los respectivos subíndices de las fórmulas y sumar los átomos que estén de un mismo lado de la ecuación.
- Verificar el balanceo final y reajustar si es necesario.
A continuación veremos los pasos a seguir para que realices un balanceo de ecuaciones químicas.
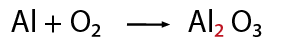
Observa que la ecuación química esté completa y bien escrita.

Para poder comprobarlo revisa las siguientes reglas:
Balanceo de un fenómeno de neutralización
A continuación analizaremos el balanceo de una ecuación química un poco más compleja, en este caso una que representa un fenómeno de neutralización, es decir, reacciona un ácido y una base, para formar una sal y agua.
- Observar que la ecuación química esté completa y bien escrita.
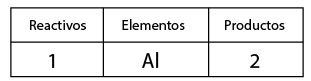
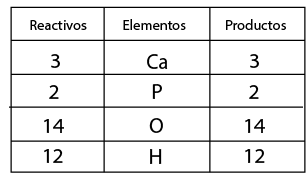
- Contar el número de elementos existentes en dicha ecuación del lado de los reactivos y después los correspondientes a los productos, empezando por: metales, no metales, dejando para el final al oxígeno e hidrógeno.
- Al hacer el conteo de cada lado, se recomienda indicar con coeficientes la igualación de la cantidad de átomos de los elementos que intervienen en la representación de una reacción química.
Ahora veamos un ejemplo:
No olvides realizar el Ejercicio 4 para que practiques el tema revisado.