Mezclas homogéneas: coloides
Los coloides son mezclas que se dan a escala microscópica, en donde las partículas de una o más sustancias se dispersan (fase dispersa) en otra sustancia llamada medio dispersor o fase dispersante (Sosa, 2007, p.22). Las partículas de la fase dispersa son suficientemente grandes como para dispersar la luz (este efecto óptico se conoce como Efecto Tyndall), pero demasiado pequeñas como para precipitar. Por tanto, una forma de distinguir una disolución de un coloide es mediante el Efecto Tyndall.

En la imagen se puede observar, en el vaso de la izquierda, dispersión de la luz porque es un coloide a diferencia del de la derecha, que no lo es.
Thomas Graham (1805-1869) propuso la palabra coloide, proveniente de la raíz griega kolas que significa “que puede pegarse”, para distinguir a este tipo de soluciones de las suspensiones y las disoluciones. Estas tres soluciones se diferencian entre sí por el tamaño de sus partículas; en las disoluciones las partículas tienen un tamaño inferior a un nanómetro de diámetro (1nm =1x10-9m es decir un milmillonésimo de metro), mientras que las partículas de los coloides tienen un diámetro entre 1nm y un micrómetro (1µm, que es igual a 1x10-6m es decir un millonésimo de metro) de diámetro. Por último, las partículas de las suspensiones tienen un tamaño mayor a 1µm de diámetro.

Una gelatina es un sol y después un gel
Graham también propuso la palabra sol para una dispersión de una sustancia sólida en un medio fluido y la palabra gel para una dispersión que tiene una estructura que le impide ser móvil. Por ejemplo, la gelatina es un sol cuando el sólido se mezcla por primera vez con agua en ebullición, pero se transforma en gel cuando se enfría (Kotz, 2005). La fase dispersa y la fase dispersora o medio dispersor, pueden ser gases, líquidos, sólidos o una combinación de diferentes fases.




Tipos de coloides
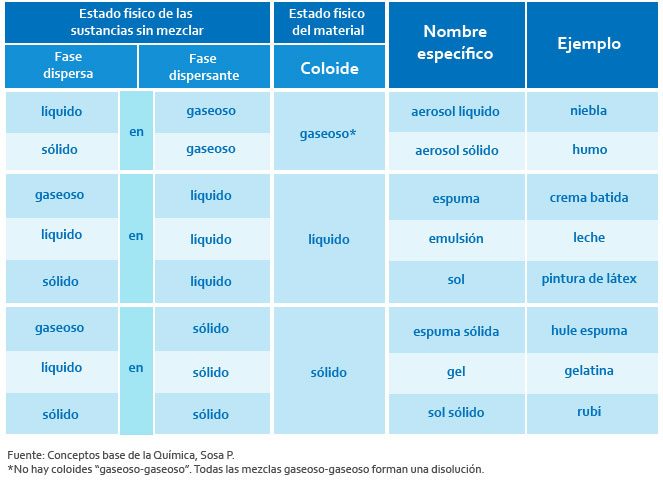
De la tabla anterior podemos destacar que, aunque las partículas de un gas puedan tener el tamaño de las de un coloide, al mezclarse con otro gas no pueden considerarse como coloide pues no hay coloides “gaseoso-gaseoso”, todas las mezclas gaseoso - gaseoso forman una disolución. Las sustancias pueden conformarse en estado coloidal excepto la mezcla gaseoso - gaseoso, por tanto, en muchos procesos naturales está implicado el estado coloidal.
Por ejemplo, investigadores de Brasil, Estados Unidos, Israel e Inglaterra, utilizaron la tecnología satelital para observar que en algunas épocas del año el viento transporta enormes cantidades de polvo (coloide tipo fase sólida en fase gaseosa) desde el desierto del Sahara - en África - hasta Sudamérica, hecho que influye en forma determinante en el ecosistema amazónico por la aportación de nutrientes que proporciona al suelo dicho polvo (Murray, 2012).
También las sustancias coloidales participan, entre otros, en la producción de pinturas, cerámica, plásticos, telas, papel fotográfico, pegamentos, tintas, cementos, hule, cuero, jabones, lubricantes, detergentes, adhesivos, insecticidas para la agricultura, condimentos alimenticios, mantequilla, queso y otros productos alimenticios.
Ahora solo te falta conocer las mezclas homogéneas denominadas suspensiones.